Siguiente: Ecuaciones de estado Subir: Condiciones para el equilibrio Anterior: Condiciones para el equilibrio
Como estamos interesados en procesos asociados con los cambios en los
parámetros extensivos, trabajamos frecuentemente con la forma diferencial
para la ecuación fundamental
![]() :
:
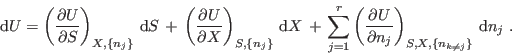
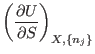 |
|
|
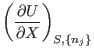 |
|
|
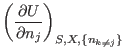 |
|
Como veremos, estas definiciones concuerdan con las nociones que teníamos
respecto de ![]() y
y ![]() . Con estas asociaciones podemos reescribir
. Con estas asociaciones podemos reescribir
Identificamos en esta expresión
![]() (
(
![]() en el caso de un
gas), de modo que para números de moles constantes tenemos
en el caso de un
gas), de modo que para números de moles constantes tenemos
Los últimos términos de la expresión completa para ![]() (
(
![]() )
representan el aumento de la energía interna asociado con el ingreso de
materia al sistema.
)
representan el aumento de la energía interna asociado con el ingreso de
materia al sistema.
Gustavo Castellano 12/06/2018