Siguiente: Equilibrio químico Subir: Condiciones para el equilibrio Anterior: Equilibrio mecánico
Veamos ahora el caso en que el pistón está fijo y además de ser diatérmico
es permeable a un tipo de partículas; para fijar ideas elegimos las de tipo 1 (![]() ). En el equilibrio, nuevamente exigimos que la entropía tome un valor máximo; en este caso, una variación infinitesimal será
). En el equilibrio, nuevamente exigimos que la entropía tome un valor máximo; en este caso, una variación infinitesimal será
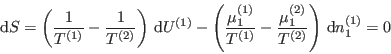
![$T^{(1)} =T^{(2)}\rule[-1.6em]{0em}{4em}$](img129.png) y
y
![$\mu^{(1)}_1=\mu^{(2)}_1\rule[-1.6em]{0em}{4em}$](img138.png)
Vemos que, así como la temperatura puede pensarse como un potencial
en cuanto al flujo de calor y la presión como potencial para cambios
de volumen, el potencial químico puede interpretarse como un potencial para el flujo de materia: una diferencia en el potencial
químico provee una ``fuerza generalizada'' que hace fluir la materia para
equilibrar los potenciales. Para verificar en qué dirección ocurre el flujo
de materia podemos suponer
![]() , y (como en el análisis sobre
flujo de calor) pensamos en un apartamiento pequeño desde el equilibrio. Como
la entropía busca el máximo,
, y (como en el análisis sobre
flujo de calor) pensamos en un apartamiento pequeño desde el equilibrio. Como
la entropía busca el máximo,
Gustavo Castellano 12/06/2018